Gestionarea deșeurilor de medicamente psihotrope și stupefiante
Data:
05/12/2017
farmacie
Farm. Rodica Aluaș
Un caz particular în cadrul farmaciei comunitare îl reprezintă deșeurile de medicamente psihotrope și stupefiante.
În concordanță cu termenii și definițiile din Convenţia unică asupra substanţelor stupefiante din 1961, la care România a aderat prin Decretul nr. 626/1973, şi Convenţia asupra substanţelor psihotrope din 1971, la care România a aderat prin Legea nr. 118/1992, avem:
- substanţă psihotropă - termen desemnând substanţele înscrise în anexele la Convenţia asupra substanţelor psihotrope din 1971;
- substanţă stupefiantă - termen desemnând substanţele înscrise în anexele la Convenţia unică din 1961 a Naţiunilor Unite asupra substanţelor stupefiante, modificată prin Protocolul din 1972;
- plante şi substanţe aflate sub control naţional - termen desemnând plantele şi substanţele cu proprietăţi psihoactive, introduse în anexele legii 143/2000, prin procedura naţională prevăzută la art. 8 alin. (3);
Deșeurile sunt acele substanțe sau obiecte pe care deținătorul le înlătură sau are intenția sau obligația de a le înlătura, dintre care unele pot fi refolosibile1.
Aceste medicamentele sau substantele chimice vor fi considerate deșeuri atunci când sunt iesite din termenul de valabilitate, sunt produse cu deficienţe care reclamă eliminarea lor din circuitul de comercializare si medicamentele stupefiante şi psihotrope returnate de la pacienţi.
Etapele privind gestionarea acestor deșeuri parcurg traseul specific deșeurilor, respectiv de manipulare (de identificare, izolare si depozitare), transport si eliminare finală. Toate etapele se regasesc în prevederile legale în vigoare.
Prevederile legale în vigoare 2, stipuleaza că :
- Unităţile farmaceutice au obligaţia să respecte prevederile legale privind retragerea din consum a medicamentelor necorespunzătoare.
- Orice unitate de producţie sau de distribuţie a medicamentelor procedează la distrugerea medicamentelor necorespunzătoare calitativ sau expirate, în acord cu reglementările în vigoare; medicamentele stupefiante şi psihotrope sunt distruse în conformitate cu legislaţia în vigoare.
Eliminarea finală se va face prin incinerare, conform reglementarilor Ordinului nr. 756 din 26 noiembrie 2004 pentru aprobarea Normativului tehnic privind incinerarea deşeurilor, în vigoare.
Legislația aplicabilă, în vigoare, privind regimul stupefiantelor si psihotropelor este Legea 339 din 2005, completată și actualizată prin3:
- OUG pentru modificarea art. 1 din Legea nr. 143/2000 privind prevenirea şi combaterea traficului şi consumului ilicit de droguri, precum şi a art. 8 din Legea nr. 339/2005 privind regimul juridic al plantelor, substanţelor şi preparatelor stupefiante şi psihotrope, Monitorul Oficial 855/2011
- HG 575/2010 - pentru actualizarea anexei la Legea nr. 339/2005 privind regimul juridic al plantelor, substanţelor şi preparatelor stupefiante şi psihotrope, precum şi a anexei la Legea nr. 143/2000 privind prevenirea şi combaterea traficului şi consumului ilicit de droguri 22 iulie 2010 Monitorul Oficial 509/2010
- OUG 6/2010 - pentru modificarea şi completarea Legii nr. 143/2000 privind prevenirea şi combaterea traficului şi consumului ilicit de droguri şi pentru completarea Legii nr. 339/2005 privind regimul juridic al plantelor, substanţelor şi preparatelor stupefiante şi psihotrope 15 februarie 2010 Monitorul Oficial 100/2010
- HG 282/2008 - pentru completarea tabelului I din anexa la Legea nr. 339/2005 privind regimul juridic al plantelor, substanţelor şi preparatelor stupefiante şi psihotrope 18 martie 2008 Monitorul Oficial 206/2008
Punerea în aplicare a Legii 339/2005 este reglementată prin HG nr. 1915 din 22 decembrie 2006
pentru aprobarea Normelor metodologice de aplicare a prevederilor Legii nr. 339/2005 privind regimul juridic al plantelor, substanţelor şi preparatelor stupefiante şi psihotrope.
De asemeni, se va tine cont și de prevederile Legii 143/2000, privind prevenirea şi combaterea traficului şi consumului ilicit de droguri, republicată în anul 2014, Monitorul Oficial nr.163 din 6 martie 2014, cu actualizările și completările ei.
Deșeurile de medicamente psihotrope și stupefiante din farmaciile comunitare provin din:
- Produsele sau substanţele psihotrope și stupefiante necorespunzătoare / neconforme (deteriorate sau expirate)
- Medicamentele care conţin substanţe stupefiante sau psihotrope retrase sau blocate de la comercializare ( pot fi fracții rămase pe stocurile farmaciilor în urma unor procese de retragere/rechemare a unor loturi de produse)
- Medicamentele care conţin substanţe stupefiante sau psihotrope, obţinute pe bază de prescripţie medicală, rămase neutilizate, returnate de către pacienți, pe baza unui proces- verbal de predare-primire4, în vederea distrugerii lor.
ETAPELE GESTIONĂRII DEȘEURILOR DE MEDICAMENTE PSIHOTROPE ȘI STUPEFIANTE
Prima etapă este reprezentată de manipularea acestor produse în incinta farmaciilor comunitare, respectiv preluarea lor (în cazul celor returnate de catre pacienți sau aparținători), identificarea, inventarierea lor, colectarea si ambalarea în vederea depozitării temporare.
În cazul produselor preluate de la pacienți, preluarea se face pe baza de proces verbal de predare-primire, întocmit in trei exemplare, cu urmatoarea destinație: un exemplar rămâne la farmacie, un exemplar, la persoana care a returnat medicamentele și un exemplar le insoțește până la distrugerea acestora.
Indiferent de modelul de proces verbal utilizat, acesta va conține obligatoriu cel putin următoarele date:
- Date complete despre cel care predă medicamentele – nume, prenume, date de identificare ( cel puțin actul de identitate), date de contact ( adresa, număr de telefon) , calitatea în care predă ( pacient sau aparținător)
- Date despre unitatea care preia medicamentele – denumire, date de identificare fiscală, date de contact- și date de identificare a farmacistului care le preia – cel puțin nume și prenume.
- Date despre medicamente – Denumire comercială, forma de prezentare, concentrația, cantitatea, serie și lot, data de valabilitate.
- Motivul returnării
- Data încheierii procesului verbal
- Semnăturile celor implicați, ștampila unității farmaceutice
Câteva sfaturi practice la preluarea stupefiantelor și psihotropelor în farmacie:
- Solicitați exemplarul pacientului de la rețeta cu care au fost ridicate produsele din farmacie. Aceasta este dovada că persoana care predă aceste stupefiante se află legal în posesia lor.
- Verificați numarul de pastile/fiole în fața aparținătorului/pacientului, concordanța seriei/lotului de pe ambalajul secundar și primar ( blistere/fiole) și sigilați cutia in fața lor.
- Daca sunt mai multe produse, le puneți intr-o cutie mai mare pe toate și o sigilați.Atașați cutiei astfel sigilate un exemplar din procesul verbal, care va însoți produsele până la distrugere.
În cazul produselor existente în farmacie, identificarea și inventarierea produselor neconforme, expirate, deteriorate sau retrase de la comercializare, se va face prin verificarea atentă a concordanței stocurilor scriptice cu cele faptice – în cazul alertelor din sistemul informatic privind produsele expirate sau retrase - sau prin inventariere parțială, cu frecvență stabilită de fiecare farmacie în parte, conform procedurilor RBPF. Colectarea lor se va face la identificare sau cel puțin lunar.
Produsele sau substanţele psihotrope si stupefiante necorespunzătoare (deteriorate sau expirate) se depozitează cu frecvență lunară în cutii sigilate, însoțite de o listă generată de programul informatic de gestiune și de procesul verbal de scoatere din gestiune/mutare gestiune expirate.
Depozitarea acestor deșeuri se va face în spaţiul destinat exclusiv acestui scop, spatiu distinct amenajat în condiții de siguranță conform depozitării produselor stupefiante, în zonele de depozitare pentru deşeuri periculoase.
Depozitarea produsele returnate de la pacienți se va face într-un spațiu distinct , unde să fie respectate toate prevederile legale: sa nu intre în contact cu produsele conforme și să fie îndeplinite toate condițiile de siguranță. Acest lucru presupune și condiția de a nu tranzita depozitul farmaciei.
În vederea trecerii la etapele următoare – predarea în vederea transportului și distrugerea efectivă – se va solicita Aprobarea de distrugere a produselor psihotrope și stupefiante neconforme, conform: Art. 48 - Distrugerea substanţelor şi preparatelor identificate ca necorespunzătoare calitativ de către persoana juridică autorizată sau de Agenţia Naţională a Medicamentului, după caz, cu termen de valabilitate expirat ori care au fost returnate, se efectuează de către o societate autorizată, în baza aprobării de distrugere emise de Ministerul Sănătăţii şi în prezenţa unei comisii constituite în condiţiile prevăzute în normele metodologice de aplicare a prezentei legi5.
Pentru obținerea autorizației de distrugere se va depune o cerere la Ministerul Sănătății, Direcția Generală Strategii și Politica Medicamentului, însoțită de următoarele documente:
Voi detalia aspecte specifice fiecăruia dintre aceste documente. Astfel :
În prima fază se trimite pe mail toată documentația cerută, inclusiv tabelele completate - scanate (semnate și ștampilate) și în format excel (2003), și se așteapta verificarea lor. Adresa de mail unde se trimit este : stupefiante@ms.ro. Pentru informații se poate apela serviciul special stupefiante la nr. de telefon: 021.307.2541
Dosarul în format scris pe hârtie se trimite la MS : MINISTERUL SĂNĂTĂȚII, DIRECŢIA GENERALĂ STRATEGII ŞI POLITICA MEDICAMENTULUI , Intr. Cristian Popişteanu, nr. 1-3, sector 1,cod 010024, Bucureşti, eventual cu mențiunea: „Conține documentație solicitare aprobare distrugere stupefiante”.
După primirea autorizației de distrugere se va trece la a doua etapă, respectiv predarea deșeurilor în vederea transportului la locul de eliminare finală.
Predarea se va face pe baza unui proces verbal de predare-primire între unitatea farmaceutică și societatea auturizată pentru distrugerea finală, unde se vor mentiona date complete d eidentificare a celor doua societăți, datele persoanelor care preda, respective preia, cantitatea de deșeuri predate, numarul autorizației de distrugere, specificația că este vorba despre deșeuri de medicamente cu regim special, lista produselor. Se datează și se semnează.
Societăţile autorizate pentru distrugerea plantelor, substanţelor şi preparatelor stupefiante şi psihotrope pot transporta şi depozita numai cantităţile specificate în aprobarea de distrugere eliberată solicitantului de către Ministerul Sănătăţii Publice.
Transportul se realizează în condiţii de securitate şi ambalare stricte, impuse de Normele privind Transportul Deşeurilor periculoase pe Drumurile Publice, conform Convenţiei A.D.R. (Acordul european referitor la transportul internaţional rutier al mărfurilor periculoase) și , fiind vorba de produse cu regim special, de legislația specifică în vigoare.
Deșeurile vor fi însoțite de „Formularul de identificare pentru transport şi eliminare finală”. Indiferent de modul de tipărire a acestui formular, va conține următoarele câmpuri:
Exemplarul 1, semnat de producător şi transportator, rămâne la producător; Exemplarul 2, semnat de producător, transportator şi de agentul economic care asigură eliminarea finală, rămâne la agentul economic; Exemplarul 3, semnat de producător, transportator şi agentul economic care asigură eliminarea finală, se trimite la producător.
Eliminarea finală, ceea de-a treia etapă din gestionarea deșeurilor din medicamente și substanțe psihotrope și stupefiante se efectuează la sediul societății autorizate, în prezenţa unei comisii constituite în condiţiile prevăzute în normele metodologice de aplicare a legii 339/2005, respectiv „Comisia pentru distrugerea plantelor, substanţelor şi preparatelor stupefiante şi psihotrope este constituită din câte un reprezentant al Ministerului Sănătăţii Publice sau desemnat de acesta la nivel local, al societăţii comerciale ce efectuează distrugerea şi al formaţiunii teritoriale a poliţiei antidrog”7.
Păstrarea evidențelor privind eliminarea finală a deșeurilor de medicamente sau substante psihotrope este reglemnată de către directiva 2008/98/ce a parlamentului european și a consiliului, din din 19 noiembrie 2008, care specifică la Art.35 (2)„ În cazul deșeurilor periculoase, evidența se păstrează timp de cel puțin trei ani, cu excepția unităților și întreprinderilor de transport de deșeuri periculoase, care trebuie să țină o evidență timp de cel puțin 12 luni. La cererea autorităților competente sau a unui deținător anterior, sunt furnizate documentele justificative conform cărora operațiunile de gestionare au fost efectuate”
În ceea ce privește stupefiantele , evidențele se păstrează timp de 5 ani , conform art. 43 din legea 339/2005.
- Copie Autorizatie de functionare
- Copie contract cu societate autorizată pentru distrugerea stupefiantelor și psihotropelor
- Tabelul cu Plantele, substanţele şi preparatele (denumirea lor comună internaţională, denumirea ştiinţifică, numele lor comun) conform tabelului nr.III (TAB III) din Legea nr 339/2005
- Tabelul cu Plantele, substanţele şi preparatele (denumirea lor comună internaţională, denumirea ştiinţifică, numele lor comun) conform tabelului nr.II (TAB II) din Legea nr 339/2005
Voi detalia aspecte specifice fiecăruia dintre aceste documente. Astfel :
- Cererea. Nu exista un model tipizat, dar, indiferent de formatul pe care îl alegeți, este recomandat să conțină cel puțin date complete de identificare a unității farmaceutice care face solicitarea, enumerarea documentelor pe care le anexați cererii . Puteți menționa că declarați pe proprie răspundere că documentele anexare în copie sunt conforme cu originalele.
- Copia Autorizatie de funcționare, semnată și ștampilată pentru conformitate cu originalul
- Copie a contractului cu o societate autorizată. Distrugerea plantelor, substanţelor şi preparatelor stupefiante şi psihotrope se realizează de către societăţile specializate care au acest obiect de activitate şi prezintă autorizaţia de funcţionare emisă de Ministerul Mediului şi Gospodăririi Apelor6. Se va acorda atenție la încheierea contractelor, astfel încât sa fie specificate concret „preluarea, transportul și distrugerea psihotropelor și stupefiantelor”, ori în contract, ori prin acte adiționale la contractual inițial.
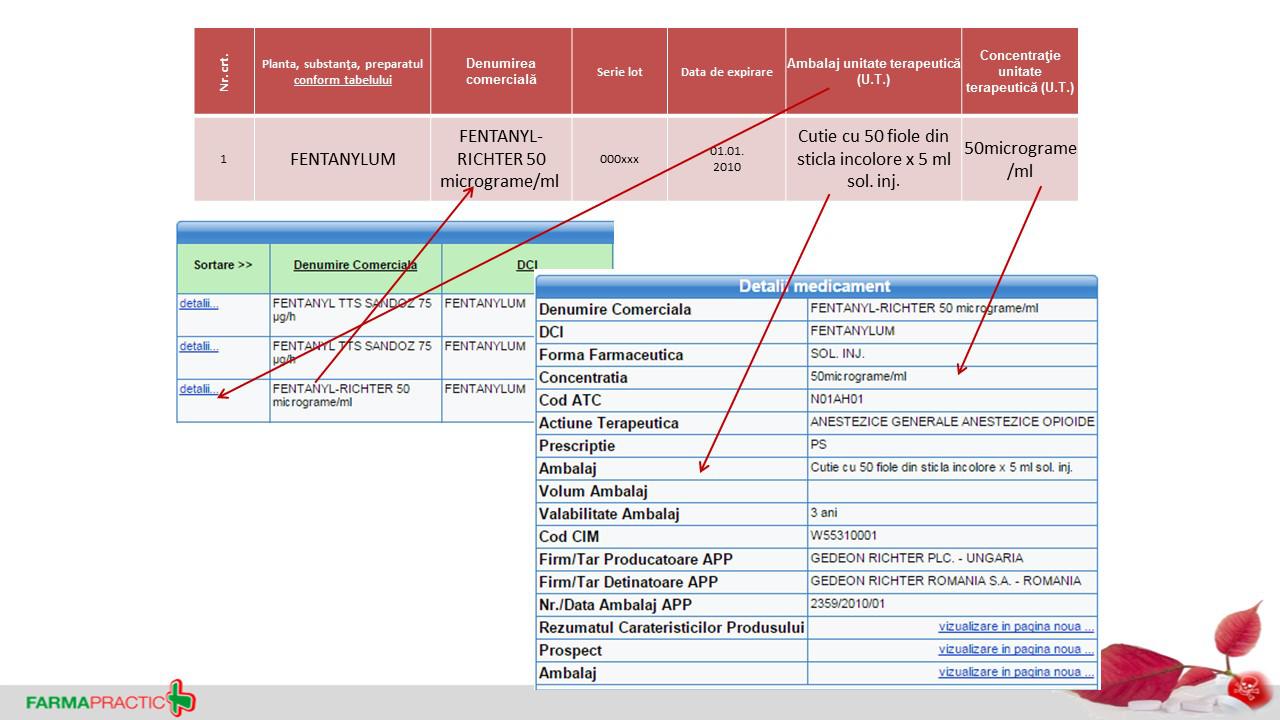
- Tabelele cu produse. Se vor intocmi separat pentru Tab.II și Tab.III. Tabelele sunt documente model ale MS, se gasesc pe site-ul ministerului. Trebuie respectat modul de completare al tabelului, iar pentru calculul final al substanțelor se folosesc tabele de calcul. În tabele se vor trece denumirile, forma farmaceutică, concentrația și descrierea produselor întocmai cu nomenclatorul Agenției Naționale a Medicamentului. Acesta se poate accesa la adresa : http://193.169.156.200/app/nom1/anm_list.asp.

- Pentru calcularea cantității se vor folosi tabelele calculator, astfel încât să fie raportată doar cantitatea de substanță activă supusă controlului.
- În tabelele trimise se va completa distinct cantitatea corespunzătoare produselor returnate de către pacienți.
În prima fază se trimite pe mail toată documentația cerută, inclusiv tabelele completate - scanate (semnate și ștampilate) și în format excel (2003), și se așteapta verificarea lor. Adresa de mail unde se trimit este : stupefiante@ms.ro. Pentru informații se poate apela serviciul special stupefiante la nr. de telefon: 021.307.2541
Dosarul în format scris pe hârtie se trimite la MS : MINISTERUL SĂNĂTĂȚII, DIRECŢIA GENERALĂ STRATEGII ŞI POLITICA MEDICAMENTULUI , Intr. Cristian Popişteanu, nr. 1-3, sector 1,cod 010024, Bucureşti, eventual cu mențiunea: „Conține documentație solicitare aprobare distrugere stupefiante”.
După primirea autorizației de distrugere se va trece la a doua etapă, respectiv predarea deșeurilor în vederea transportului la locul de eliminare finală.
Predarea se va face pe baza unui proces verbal de predare-primire între unitatea farmaceutică și societatea auturizată pentru distrugerea finală, unde se vor mentiona date complete d eidentificare a celor doua societăți, datele persoanelor care preda, respective preia, cantitatea de deșeuri predate, numarul autorizației de distrugere, specificația că este vorba despre deșeuri de medicamente cu regim special, lista produselor. Se datează și se semnează.
Societăţile autorizate pentru distrugerea plantelor, substanţelor şi preparatelor stupefiante şi psihotrope pot transporta şi depozita numai cantităţile specificate în aprobarea de distrugere eliberată solicitantului de către Ministerul Sănătăţii Publice.
Transportul se realizează în condiţii de securitate şi ambalare stricte, impuse de Normele privind Transportul Deşeurilor periculoase pe Drumurile Publice, conform Convenţiei A.D.R. (Acordul european referitor la transportul internaţional rutier al mărfurilor periculoase) și , fiind vorba de produse cu regim special, de legislația specifică în vigoare.
Deșeurile vor fi însoțite de „Formularul de identificare pentru transport şi eliminare finală”. Indiferent de modul de tipărire a acestui formular, va conține următoarele câmpuri:
- Datele de identificare a unităţii producătoare de deşeuri periculoase (denumirea completă şi adresa)
- Datele de identificare a agentului economic prestator de servicii de transport, conform contractului (denumirea completă, adresa, numărul de înmatriculare la registrul comerţului)
- Datele de identificare a agentului economic prestator de servicii de eliminare finală, conform contractului (denumirea completă, adresa, numărul de înmatriculare la registrul comerţului)
- Cantitatea de deşeuri periculoase trimisă, transportată şi eliminată (kg)
- Data şi ora predării pentru transport
- Numele (scris lizibil) şi semnătura persoanei care a predat deşeurile periculoase pentru transport
- Numele (scris lizibil) şi semnătura persoanei care a primit deşeurile periculoase pentru transport.
- Data şi ora predării pentru eliminarea finală
- Numele (scris lizibil) şi semnătura persoanei care a predat deşeurile periculoase spre eliminare
- Numele (scris lizibil) şi semnătura persoanei care a primit deşeurile periculoase spre eliminare
- Data şi ora eliminării finale
- Procedura de eliminare finală utilizată
- Numele (scris lizibil) şi semnătura persoanei responsabile din partea agentului economic care efectuează eliminarea deşeurilor periculoase.
Exemplarul 1, semnat de producător şi transportator, rămâne la producător; Exemplarul 2, semnat de producător, transportator şi de agentul economic care asigură eliminarea finală, rămâne la agentul economic; Exemplarul 3, semnat de producător, transportator şi agentul economic care asigură eliminarea finală, se trimite la producător.
Eliminarea finală, ceea de-a treia etapă din gestionarea deșeurilor din medicamente și substanțe psihotrope și stupefiante se efectuează la sediul societății autorizate, în prezenţa unei comisii constituite în condiţiile prevăzute în normele metodologice de aplicare a legii 339/2005, respectiv „Comisia pentru distrugerea plantelor, substanţelor şi preparatelor stupefiante şi psihotrope este constituită din câte un reprezentant al Ministerului Sănătăţii Publice sau desemnat de acesta la nivel local, al societăţii comerciale ce efectuează distrugerea şi al formaţiunii teritoriale a poliţiei antidrog”7.
Păstrarea evidențelor privind eliminarea finală a deșeurilor de medicamente sau substante psihotrope este reglemnată de către directiva 2008/98/ce a parlamentului european și a consiliului, din din 19 noiembrie 2008, care specifică la Art.35 (2)„ În cazul deșeurilor periculoase, evidența se păstrează timp de cel puțin trei ani, cu excepția unităților și întreprinderilor de transport de deșeuri periculoase, care trebuie să țină o evidență timp de cel puțin 12 luni. La cererea autorităților competente sau a unui deținător anterior, sunt furnizate documentele justificative conform cărora operațiunile de gestionare au fost efectuate”
În ceea ce privește stupefiantele , evidențele se păstrează timp de 5 ani , conform art. 43 din legea 339/2005.
1 Legea nr. 211/2011 privind regimul deşeurilor
2 Legea 95 /2006, actualizată până la 6 aprilie 2017, art. 872
3 http://legeaz.net/legea-339-2005-stupefiante/pagina-2
4 Legea 339 din 2005, art.38(3) și OMS 1915/2006, art.39(2)
5 Legea 339 din 29 noiembrie 2005, privind regimul juridic al plantelor, substanţelor şi preparatelor stupefiante şi psihotrope
6 HG Nr. 1915 din 22 decembrie 2006, pentru aprobarea Normelor metodologice de aplicare a prevederilor Legii nr. 339/2005 privind regimul juridic al plantelor, substanţelor şi preparatelor stupefiante şi psihotrope, art.51
7 HG Nr. 1915 din 22 decembrie 2006, pentru aprobarea Normelor metodologice de aplicare a prevederilor Legii nr. 339/2005 privind regimul juridic al plantelor, substanţelor şi preparatelor stupefiante şi psihotrope, art.53
Prof. dr. Gabriel Hancu
Universitatea de Medicină, Farmacie, Științe și Tehnologie din Tîrgu Mureș
Facultatea de Farmacie, Disciplina Chimie farmaceutică
Universitatea de Medicină, Farmacie, Științe și Tehnologie din Tîrgu Mureș
Facultatea de Farmacie, Disciplina Chimie farmaceutică
punctul pe i
2024 a debutat în lumea farmaceutică cu histeria eliberării antibioticelor. Presa prost informată, ca de obicei, a amplificat problema, iar pacienții nu au înțeles nimic, poate nici unii dintre farmaciști sau medicii prescriptori. Ordinul Ministerului Sănătății, menit să reglementeze eliberarea antibioticelor în România, a stârnit dezbateri aprinse cu privire...
...
dr. farm. Marian Pană
orizonturi
Contribuția mea este minimală pentru acest articol. M-am gândit ca este bine să știm cu toții despre strategia națională de sănătate pentru perioada 2023 – 2030, aprobată prin HG (hotărâre guvern) nr. 1.004 din 20 octombrie 2023 (actul legislativ este postat pe site, la sectiunea Legislație/Hotărâri de Guvern).
...09/06
09/06

Acest site, numele sau si tot materialul inclus este copyright ©
Colegiul Farmacistilor din Romania
(toate drepturile rezervate).
Reproducerea totală sau parțiala, și sub orice altă formă, tipărită sau electronică, sau distribuția articolelor se face numai cu acordul scris al autorului.
WebDesign by Incorom
Reproducerea totală sau parțiala, și sub orice altă formă, tipărită sau electronică, sau distribuția articolelor se face numai cu acordul scris al autorului.
WebDesign by Incorom


