Am scris câteva articole în care am vorbit și despre acest subiect.
Acum mi-am propus sa fiu scurt si clar și să mă concentrez doar pe structura prețului medicamentului.
Structură preț medicament în Europa
- sunt precizări importante în rapoartele The Pharmaceutical Industry in Figures – Key Data din anii 2019, 2024 și 2025 publicate de EFPIA (European Federation of Pharmaceutical Industries and Associations).
- am lăsat ca atare -textul în limba engleză- despre Price Structure(Structura de preț)
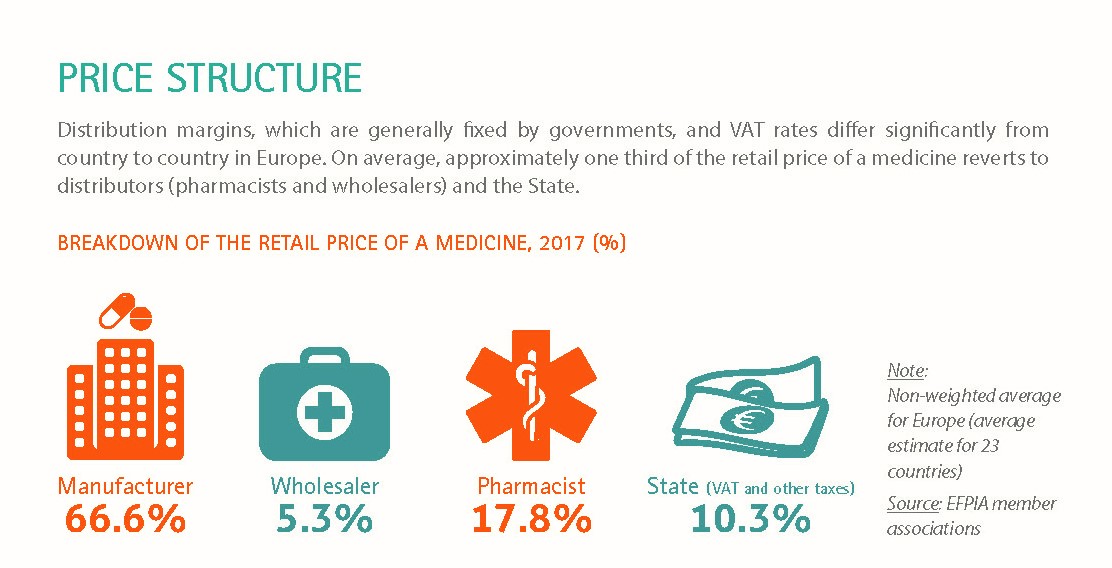
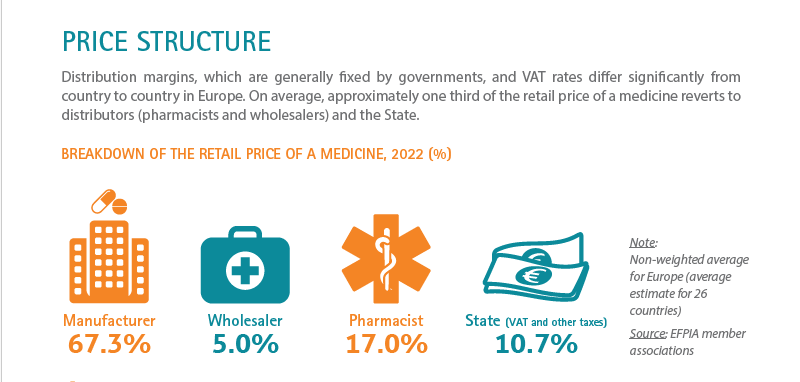

Structura prețului unui medicament are patru componente care se adresează celor patru „jucători” implicați:
- producător
- distribuitor
- farmacist
- stat (TVA)
Se observă că farmacia europeană primește în medie -pentru motive clare și evidente- peste 17% din prețul medicamentului.
Structură preț medicament în România
Iată ce prevede OMS 368/2017 cu privire la actualul sistem de adaosuri, aplicabil pentru medicamentele Rx, în farmacii:
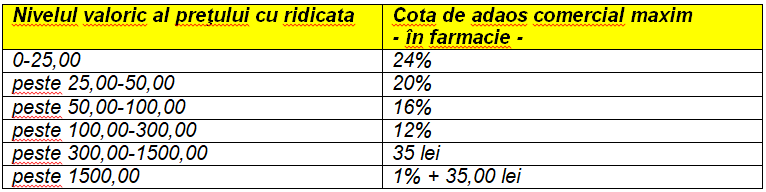
Sistemul de adaosuri reprezintă sursa de venit utilizată pentru farmaciile comunitare din România.
Valorile privind cotele de adaos comercial sunt aceleași din anul 2009!
Pe baza tabelului de mai sus am construit un alt tabel, cu exemple de preț ale unor medicamente Rx pe fiecare nivel valoric, din care reies componentele procentuale (%) care revin „jucătorilor” implicați, adică structura de preț:
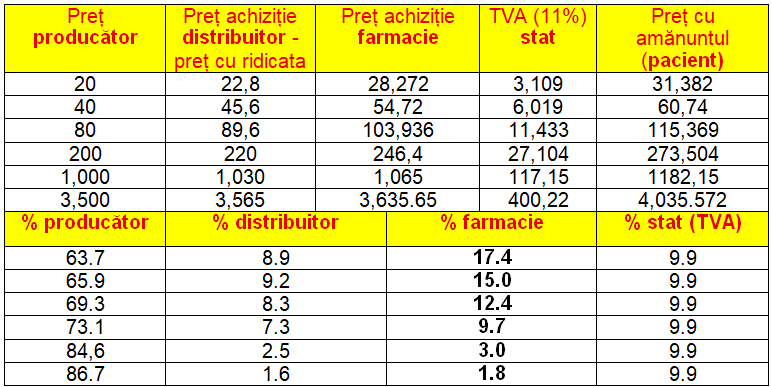
Când faci efectiv calculele, realizezi cât de departe suntem de Europa în acest domeniu!
Este evident că trebuie actualizate valorile privind cotele de adaos comercial la primele cinci nivele valorice din acest Ordin.
Rămane o discuție separată ce hotărâm cu privire la cota de adaos comercial pentru al șaselea nivel valoric (preț cu ridicata >1,500 lei).
De asemena, presupun că trebuie -cel puțin- un nou nivel valoric (preț cu ridicata >10,000) lei, cu cota de adaos comercial aferentă, care ar fi reprezentat de sute de medicamente (vedeți ultimul Canamed).
Așa cum am spus de nenumărate ori, “economicul bate farmaceuticul”. În loc să ne focalizăm -numai- pe pacienți, suntem nevoiți să acordăm atenție și timp semnificativ zonei comerciale.
Este absolut necesar să construim un sistem de adaosuri rezonabil care să asigure viabilitatea financiară a farmaciei comunitare ceea ce înseamnă salarii/venituri decente pentru farmaciști.
Dacă începutul anului 2026 ar avea un motto în sănătate, acesta ar putea fi: „Stabilitate prin actualizări succesive”. Exact ca în viață ... ...
În urmă cu 20 de ani, conform expunerii de motive a proiectului de lege respectiv care prevedea instituirea taxei pe “viciu”, destinaţia veniturilor colectate ... ...

WebDesign by Incorom


